Processo Produttivo
Ricerca e Sviluppo
I fattori critici di successo del Gruppo sono l’adeguatezza della gamma dei prodotti che offriamo e la capacità di innovarla continuamente per andare incontro alle esigenze del mercato e per crearne di nuove.
Il nostro posizionamento su prodotti ad alta tecnologia e il contesto competitivo globale in cui esso opera comportano un impegno continuo e rilevante in termini di ricerca e sviluppo di nuovi prodotti e nuove tecnologie; ciò che ci caratterizza è la capacità di pensare in maniera unica, di innovare considerando le esigenze del medico e del paziente nel settore medicale piuttosto che del cliente in quello industriale, partendo da ogni intuizione che possa scaturire dall’osservazione costante e profonda di problemi che non hanno ancora soluzione.
Sono le competenze maturate e la passione delle nostre persone a fare la vera differenza; Il Gruppo El.En. e le persone che vi lavorano vantano infatti una conoscenza dei fenomeni fisici, biomedicali e tecnologici maturata in quarant’anni di esperienza, che porta ad una spiccata capacità di innovare il proprio know-how, le tecnologie di produzione, i processi, i prodotti e i servizi correlati.
Il Gruppo organizza la propria attività di ricerca e sviluppo secondo linee programmatiche e con una visione a medio/lungo termine, in modo da approntare tempestivamente e con continuità prodotti innovativi nelle prestazioni e nelle applicazioni. Nelle attività di ricerca condotte nei nostri laboratori, così come mediante la collaborazione con importanti centri di ricerca, ospedali ed università, sia a livello nazionale che internazionale, non ci poniamo limiti, spinti dal desiderio e dalla passione per tutto ciò che è oppure che può divenire nuovo.
La ricerca svolta è di tipo applicato per la maggior parte delle attività, mentre è di base per alcuni argomenti specifici, generalmente legati ad attività riguardanti obiettivi innovativi a medio e a lungo termine. La capacità di innovare del Gruppo El.En. è dimostrata anche dal numero di brevetti che le società del Gruppo hanno depositato: in meno di quarant’anni, sono 128 i brevetti depositati, mentre più di 80 sono ad oggi in fase di domanda.

Qualità e sicurezza del prodotto
Il Gruppo è consapevole che la complessità del suo business richiede alti standard qualitativi e per questo l’impegno che promuoviamo e portiamo avanti nei confronti della Qualità e della Sicurezza dei nostri prodotti è essenziale per garantirne la continua crescita e il successo. Poniamo sempre la massima attenzione alle fasi di design e di sviluppo dei nostri sistemi; il nostro valore passa infatti anche attraverso lo studio e l’applicazione di metodiche sempre più selettive, efficaci e sicure.
Ci impegniamo ogni giorno a fornire prodotti di valore ai nostri clienti al fine di instaurare un processo di fidelizzazione basato su qualità, affidabilità e sicurezza, e per garantire che tali requisiti di prodotto siano riconosciuti e apprezzati e che sia adottata ogni azione necessaria a garantirne le conformità legislative.
A questo scopo alcune società del Gruppo si sono dotate di un “Manuale Sistema di Gestione Integrata”, che risponde ai requisiti del TUSSL n. 81 del 2008, per descrivere gli obiettivi e le politiche del Sistema di Gestione per la Qualità e le modalità con le quali si applica. Il manuale definisce i criteri generali affinché siano soddisfatti i requisiti di sicurezza e di prestazioni dei prodotti durante tutto il loro ciclo di vita così come dei servizi forniti. Le società El.En. S.p.A., Deka M.E.L.A. S.r.l., Quanta System S.p.A., ASA S.r.l. e Asclepion GmbH si sono dotate di una Politica per la Qualità che garantisce la conformità delle attività alle norme degli Enti nazionali degli Stati in cui opera.
Le diverse società del Gruppo ottemperano, in funzione dell’area geografica e della tipologia di business in cui operano, ai seguenti standard e normative:
ISO 9001;
ISO 13485 relativa al sistema di gestione qualità per dispositivi medici;
Direttiva Europea MDD93/42/EEC (Medical Devices Directive) che a breve sarà sostituita dal Regolamento Europeo (UE) 2017/745 MDR (Medical Device Regulation);
Leggi nazionali degli stati membri della Comunità Europea e degli Stati Extra-europei come ad esempio gli Stati uniti D’America (21CFR820/803/806), Giappone, Cina (CCC- Certificazione per componenti elettronici e Enterprise standard “CNC laser cutting machine”) e Brasile.
Le società El.En. S.p.A., Deka Mela S.r.l., Quanta System S.p.A., Asclepion GmbH e ASA S.r.l. hanno ottenuto nel corso degli ultimi due anni la certificazione MDSAP (Medical Device Single Audit Program). Tale certificazione permette ad organismi riconosciuti e accreditati dalle Autorità Regolatorie dei cinque paesi aderenti (U.S.A., Canada, Brasile, Giappone e Australia) di condurre un unico audit presso i fabbricanti di dispositivi medici per verificare che questi ultimi soddisfino i requisiti della ISO 13485 e le deviations nazionali dei Paesi di riferimento.
Le stesse società si stanno organizzando per ottenere la certificazione CE secondo l’allegato IX del nuovo Regolamento Europeo sui dispositivi medici UE 2017/745 MDR. Tale certificazione, che entrerà in vigore entro la metà del 2021, andrà a sostituire definitivamente la precedente Direttiva 93/42/ECC, che rimarrà comunque valida fino al 2024.
Il nuovo regolamento inserirà severi e stringenti requisiti riferiti a:
- Valutazione clinica dei dispositivi medici, dimostrare l’efficacia clinica del dispositivo attraverso indagini o analisi della bibliografia disponibile di prodotti similari;
- Reprocessing dei dispositivi medici (pulizia, disinfezione, sterilizzazione, etc...);
- Post market surveillance PMS (vigilanza per incidenti ed eventi avversi sul mercato);
- Post market clinicalfollow up PMCF (rivalutazione periodica di sicurezza ed efficacia clinica).
Inoltre il Regolamento prevede un nuovo sistema di tracciabilità UDI (Unique Device Identification), simile all’FDI americano, di tutti i dispositivi immessi in commercio, nonché l'identificazione e tracciabilità di tutti gli operatori economici (fabbricante, importatore, distributore). Al fine di garantire maggiore qualità e conformità del prodotto, il nuovo regolamento introduce e obbliga i fabbricanti a nominare una nuova figura aziendale quale responsabile della conformità regolatoria del prodotto rilasciato sul mercato, e della sua documentazione tecnica di certificazione.
Il Gruppo si impegna a raggiungere, attraverso la motivazione e il coinvolgimento delle proprie persone, un miglioramento continuo della qualità dei propri prodotti e servizi; questo obiettivo viene perseguito attraverso l’ottimizzazione dei processi aziendali, secondo criteri di efficienza e metodi di lavoro univoci e omogenei, snelli ed efficaci. Si tende inoltre sempre di più ad una Politica di Qualità orientata alla gestione del rischio, come strumento di valutazione e di decisione, al fine di perseguire il miglioramento continuo attraverso opportune azioni preventive o correttive.
In un ambiente competitivo come quello dell’industria medicale, la competenza degli esperti che lavorano nel settore Regulatory Affairs è di notevole importanza economica per l’azienda, soprattutto se questa persegue obiettivi di internazionalizzazione nella sua strategia commerciale. All'interno delle società del Gruppo El.En. che operano nel settore medicale la funzione Regulatory documenta la conformità alle esigenze degli organismi di governo di tutelare la salute pubblica, vigilando sulla sicurezza e l’efficacia dei prodotti dell’industria di settore. Le aziende produttrici di dispositivi medici garantiscono che i loro prodotti siano in linea con le normative vigenti in materia di sicurezza. Per questo è altamente strategico dotarsi di un ufficio specializzato di esperti in Regulatory Affairs affinché si mantengano i prodotti aggiornati rispetto alle richieste di legge, si ottengano e gestiscano le certificazioni di prodotto, si assicuri il continuo mantenimento della conformità fungendo da intermediario tra le richieste delle autorità e le esigenze espresse da tutte le aree funzionali dell’azienda, seguendo l’iter documentario e mettendosi a disposizione per eventuali richieste documentali e chiarimenti aggiuntivi da parte delle istituzioni. L’attività regolatoria oggi richiede la presenza di più attori, possibilmente con diverso tipo di cultura tecnica, scientifica e amministrativa e con una ottima padronanza delle lingue, perché occorre conoscere le normative europee, quelle nazionali e anche quelle dei paesi extra europei.
Catena di fornitura
Nell'ultimo anno il valore degli acquisti a livello consolidato è stato pari a 255,2 milioni di euro mentre le lavorazioni presso terzi sono state pari a 12,6 milioni di euro. Il Gruppo El.En. ritiene che una stretta collaborazione con la propria supply chain sia essenziale per conseguire più elevati standard qualitativi del prodotto finito e più in generale dell’intero processo produttivo.
L’obiettivo finale è quello di stabilire un rapporto di cooperazione duraturo, caratterizzato da trasparenza e collaborazione. I fornitori devono possedere dei requisiti di sicurezza, qualità e solidità finanziaria, in modo da minimizzare potenziali interruzioni operative e costi imprevisti. Vengono svolte con continuità analisi e valutazioni preventive per cogliere le tendenze di mercato, monitorare l’evoluzione dei fornitori attuali e di quelli potenziali, il loro aggiornamento tecnico e la regolamentazione di settore, anche in materia di commercializzazione dei loro prodotti a noi venduti.
Il Gruppo opera in un quadro di concorrenza leale con onestà, legalità e correttezza, nel rispetto dei legittimi interessi di tutti gli stakeholder; il Codice Etico del Gruppo contiene i principi e le regole che tutti coloro che entrano in contatto con l’azienda sono tenuti a rispettare.
Nei contratti di fornitura per componenti critici sottoscritti da El.En. S.p.A., la controparte dichiara di aver ricevuto il Codice Etico e di accettarlo. In quest’ottica dunque viene chiesto ai fornitori di rispettare determinati requisiti:
- solidità finanziaria;
- esperienza acquisita nel settore;
- affidabilità;
- risorse e capacità tecniche e progettuali;
- capacità produttiva;
- adozione di sistemi di controllo di qualità e sicurezza dei prodotti, coerenti con le richieste del Gruppo.
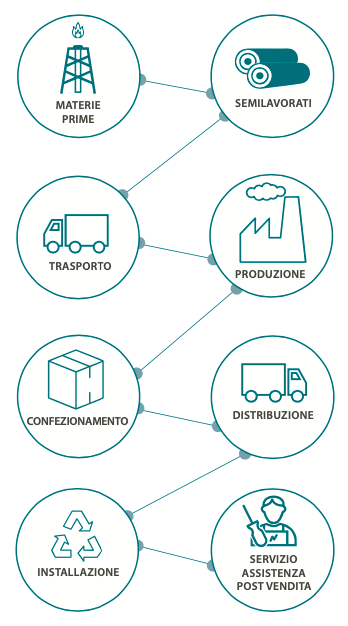
In particolare, nelle società produttive del Gruppo la selezione dei fornitori segue delle precise procedure di qualifica e approvazione per garantire la qualità del prodotto e il massimo rispetto delle tempistiche di consegna. Possono inoltre essere previsti degli audit presso il fornitore: al termine dell’analisi, in base all’esito di tutte le prove svolte, si procede ad accettare il fornitore o ad escluderlo giudicando insufficiente la sua qualità. Una volta che i fornitori sono stati giudicati qualitativamente idonei vengono comunque pianificate valutazioni periodiche per assicurare il mantenimento degli standard qualitativi richiesti: tali valutazioni prendono in considerazione aspetti quali la flessibilità, ossia la capacità di adattarsi alle esigenze dell’organizzazione, la tempestività di risposta e di gestione degli imprevisti, la struttura organizzativa e la puntualità delle consegne oltre che la valutazione della qualità della merce consegnata. Annualmente sono inoltre previste delle verifiche ispettive da tenersi alcuni fornitori da parte di auditor interni addestrati.
Come previsto all’interno del Piano di Sostenibilità, nella procedura di qualifica e approvazione dei fornitori di componenti critici* abbiamo inserito anche la valutazione di alcuni aspetti legati alle tematiche di sostenibilità, affinché anche queste contribuiscano alla valutazione complessiva del fornitore. I nuovi criteri di qualifica sono entrati a regime da questo esercizio per la Capogruppo El.En. S.p.A. e per la controllata Deka Mela S.r.l., dove il 43% dei fornitori di componenti critici è stato valutato anche secondo criteri ambientali e sociali, mentre per le controllate Asa S.r.l. e Quanta System S.p.A. tali criteri sono inseriti nella valutazione dei fornitori di componenti critici dal 2021.
* El.En. considera fornitori di componenti critici coloro che forniscono un componente/assieme che ha impatto sulla sicurezza del Paziente e/o dell'Operatore e che presenta un indice di rischio alto oppure che offrono servizi legati alla qualità del prodotto che hanno impatto sulla sicurezza del Paziente e/o dell'Operatore.